Saúde redistribui produção de biológicos entre laboratórios públicos
O Ministério da Saúde divulgou nesta segunda-feira (20), no Diário Oficial da União (DOU), a nova distribuição da produção de insumos biológicos no país por meio de Parcerias para o Desenvolvimento Produtivo (PDP). A plataforma é uma das oito lançadas em outubro do ano passado pela Nova Política de Inovação Tecnológica da pasta. O objetivo é organizar, entre Fiocruz/Biomanguinhos, Instituto Butantan e Tecpar – laboratórios com maior expertise no tema, a elaboração de produtos biológicos estratégicos para o SUS. A organização entre essas instituições de pesquisas irá facilitar o processo de fabricação de insumos para o tratamento de artrite, câncer e doenças autoimune, por exemplo. (Veja tabela abaixo)
Em 2016, foi iniciada a revisão das Parcerias para o Desenvolvimento Produtivo (PDPs). Até aquele momento, sete laboratórios públicos tinham PDPs vigentes para a produção de biológicos (MABs). Desses, apenas três, Fiocruz-Biomanguinhos, Butantan e Tecpar já eram tradicionais produtores de biológicos para o ministério da Saúde e mostraram-se promissores no desenvolvimento de tecnologia monoclonal, ou seja, a tecnologia mais avançada da indústria farmacêutica, sendo os únicos laboratórios públicos que possuem pesquisas e iniciativas nesta área de atuação.
Os demais laboratórios públicos serão especializados em outras sete plataformas: Síntese Química, hemoderivados, doenças raras, fitoterápicos, doenças negligenciadas, produtos para a saúde e medicina nuclear. O objetivo da especialização dos laboratórios por meio da Nova Política de Plataformas Inteligentes de Tecnologia em Saúde é oferecer competitividade, escala de comercialização dos produtos e capacitação dos pesquisadores. A expectativa é que haja um investimento privado de R$ 6,4 bilhões, a construção de pelo menos 3 novas fábricas, eração de mais de 7.400 vagas de empregos qualificados; além de envolver cerca de 450 doutores especializados em pesquisas para auxiliar o desenvolvimento de medicamentos e produtos para a saúde.
REVISÃO DAS PDPs – As Parcerias para o Desenvolvimento Produtivo (PDP) tiveram seus primeiros critérios definidos em 2012, na gestão do ex-ministro da Saúde, Alexandre Padilha, com o objetivo de racionalizar o poder de compra do Estado, incentivar o desenvolvimento tecnológico no país, além de focar na produção local de produtos estratégicos para o SUS. A partir daí, foram criadas normas e critérios para o estabelecimento e realização desses acordos entre as instituições públicas e entidades privadas para a transferência das tecnologias.
Em 2014, o então ministro da Saúde, Arthur Chioro divulgou o novo marco regulatório da política, em que definiu uma lista anual com produtos considerados estratégicos para o Sistema Único de Saúde (SUS), além de aprimoramento do processo de desenvolvimento produtivo na área da saúde, com definição de prazos para apresentação de propostas de transferência tecnológica, maior monitoramento do governo e garantia de segurança. Também foram definidas as fases de uma PDP, sendo a Fase III definida como início de aquisição do produto, as fases I e II são destinadas, respectivamente, a apresentação da proposta e implementação da mesma. A fase IV corresponde pela finalização do processo de transferência de tecnologia.
Finalmente em 2016, na gestão Ricardo Barros, as PDP’s foram reorganizadas visando o fortalecimento da estratégia nacional de fomento à produção industrial brasileira, criando soluções tecnológicas em saúde como forma de promover o acesso integral e reduzir a vulnerabilidade do sistema de saúde, além de promover a produtividade, a competitividade e o desenvolvimento econômico e social.
LISTA ESTRATÉGICA – Em janeiro deste ano, o Ministério da Saúde divulgou a nova lista de produtos estratégicos para o SUS. O rol consta com 52 produtos que são elegíveis para a apresentação de propostas de projetos de transferência de tecnologias no ano de 2017. Desse total, 19 são produtos biológicos que interessam ao SUS e que podem ser produzidos no Brasil.
Para a publicação dessa nova lista, o Ministério da Saúde considerou alguns critérios essenciais, como: Produtos negligenciados, Alta tecnologia, medicamentos de alto custo, produtos mais judicializados e buscou o atendimento às plataformas que foram acordadas na política do Governo Federal de incentivo ao Complexo Industrial da Saúde – biotecnologia, doenças raras, fitoterápicos, doenças negligenciadas, produtos para a saúde, hemoderivados, medicina nuclear e síntese química. A lista está aberta a sugestões e contribuições dos laboratórios e da indústria farmacêutica e estará disponível para a síntese e atualização da lista sempre que o Ministério da Saúde autorizar.
BALANÇO – O Ministério da Saúde conta com 86 parcerias de desenvolvimento produtivo vigentes, envolvendo 18 laboratórios públicos e 43 privados para o desenvolvimento de 88 medicamentos, 4 vacinas e 13 produtos da área da saúde. Em dezembro, após reunião do GECIS, foram incorporados mais 7 parcerias ao rol já existente. As PDPs têm como objetivo transferir tecnologias para a produção nacional de medicamentos, insumos e tecnologias estratégicas para a saúde. O prazo máximo para a conclusão do projeto, com a finalização da transferência de tecnologia, será de até 10 anos.
ANTICORPOS MONOCLONAIS E ETANERCEPT
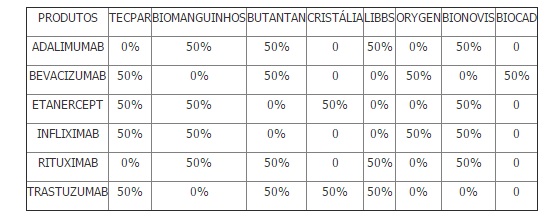
Fonte: Ascom/MS
Autor: Victor Maciel, da Agência Saúde



